两性氧化物
定义
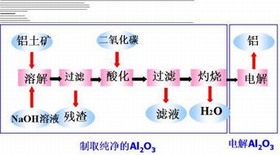 两性氧化物
两性氧化物两性氧化物是指既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物。这类氧化物在化学反应中既表现出酸性氧化物的性质,又表现出碱性氧化物的性质,其特性取决于反应环境的酸碱性。
化学性质
与酸反应(表现碱性):
两性氧化物与强酸反应生成盐和水。
例如:与碱反应(表现酸性):
两性氧化物与强碱反应生成盐(通常为含氧酸盐)和水。
例如:(生成偏铝酸钠)
常见两性氧化物
铝的氧化物:氧化铝(),常见于刚玉、铝土矿。
锌的氧化物:氧化锌(),用于防晒剂、橡胶工业。
其他元素氧化物:
氧化铅()
氧化锡()
氧化铬()
物理性质
外观:多为固体,颜色因物质而异(如为白色,为绿色)。
熔沸点:通常较高,例如熔点达2054℃,适合耐火材料。
存在形式与用途
自然界存在:
氧化铝存在于铝土矿、刚玉(红宝石、蓝宝石的主要成分)。
工业应用:
:制造金属铝、耐火材料、陶瓷。
:化妆品、医药(抗菌)、电子器件(半导体)。
与其他氧化物的区别
| 类型 | 与酸反应 | 与碱反应 | 示例 |
|---|---|---|---|
| 碱性氧化物 | 是 | 否 | |
| 酸性氧化物 | 否 | 是 | |
| 两性氧化物 | 是 | 是 |
注意事项
并非所有金属氧化物都是两性的,如(碱性)、(酸性)。
两性氧化物通常为过渡金属或主族金属(如Al、Zn、Sn等)的氧化物。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
上一篇 世界波(精彩进球的概括) 下一篇 中流砥柱
